重磅 | 尚科生物:全球首家NMN原料通过FDA NDI认证
经过美国FDA(美国食品药品监督管理局)权威机构专业委员的严格审核,2022年5月17日尚科生物医药(上海)有限公司正式收到FDA的确认函(AKL):根据FDA的NDI接受确认函信内容,到2022年6月5日静默期满后,尚科生物的NMN原料就可以正式用于美国保健品的生产、销售和推广上了。同时在2022年6月21日开始,可以在www.regulations.gov网站上作为新的膳食补充剂被找到,编号为1247。
MORE
27
2023-11
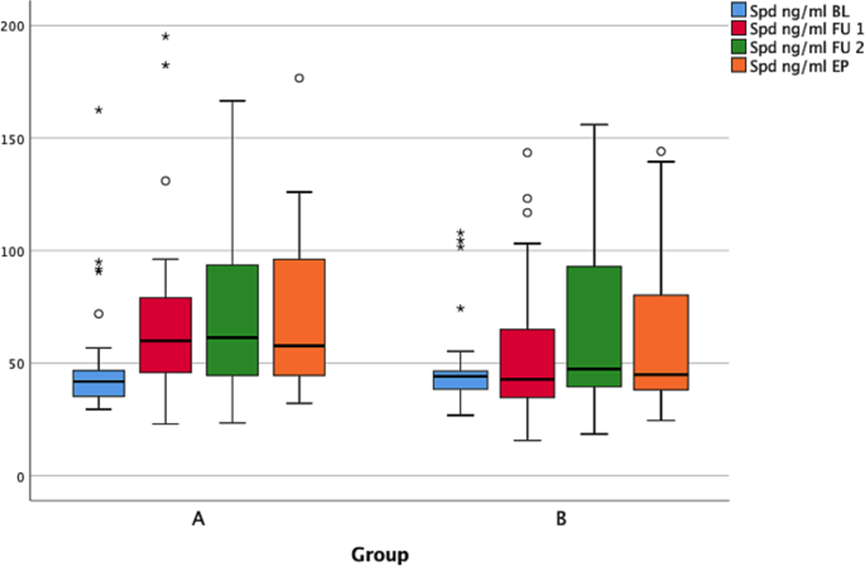
亚精胺对老年痴呆患者的积极作用
世界卫生组织(WHO)统计,全世界包括阿尔茨海默病(AD)在内的痴呆症患者已经达到了5000万人,预计到2050年将增至1.52亿人。
20
2023-10
尚科生物荣获“合成生物学新锐企业”奖项
2023年10月19日,由临港集团和蒲公英共同举办的“2023上海国际生物医药产业周合成生物学科技创新产业大会”在上海临港生命蓝湾进行。尚科生物医药(上海)有限公司荣获“2023合成生物学新锐企业”奖项,公司总经理还在会上进行了路演,向参会嘉宾介绍尚科生物的情况。
11
2023-09
携手同行 共赢未来 | 尚科生物与彼特化工签订战略合作协议
尚科生物衷心感谢所有合作伙伴的支持与信任,希望有更多的伙伴一起携手同步,以绿色科技守护生命健康,创造美好生活!
16
2023-08
生物工程学科发展战略研讨会圆满收官!
2023年8月11-13日,由华东理工大学主办的“生物工程学科发展战略研讨会暨第一届生物反应器工程与生物制造学术会议”在上海隆重召开。
10
2023-08
金鸡湖畔,共聚第五届中国国际生物&化学制药博览会
第五届中国国际生物&化学制药博览会圆满举办。
上一页
1
2
...
5
下一页
重磅 | 尚科生物:全球首家NMN原料通过FDA NDI认证
经过美国FDA(美国食品药品监督管理局)权威机构专业委员的严格审核,2022年5月17日尚科生物医药(上海)有限公司正式收到FDA的确认函(AKL):根据FDA的NDI接受确认函信内容,到2022年6月5日静默期满后,尚科生物的NMN原料就可以正式用于美国保健品的生产、销售和推广上了。同时在2022年6月21日开始,可以在www.regulations.gov网站上作为新的膳食补充剂被找到,编号为1247。
Read more >>
尚科生物荣获“合成生物学新锐企业”奖项
2023年10月19日,由临港集团和蒲公英共同举办的“2023上海国际生物医药产业周合成生物学科技创新产业大会”在上海临港生命蓝湾进行。尚科生物医药(上海)有限公司荣获“2023合成生物学新锐企业”奖项,公司总经理还在会上进行了路演,向参会嘉宾介绍尚科生物的情况。
Read more >>
邀请函 | 尚科生物邀您共赴2023CPHI展会
Read more >>
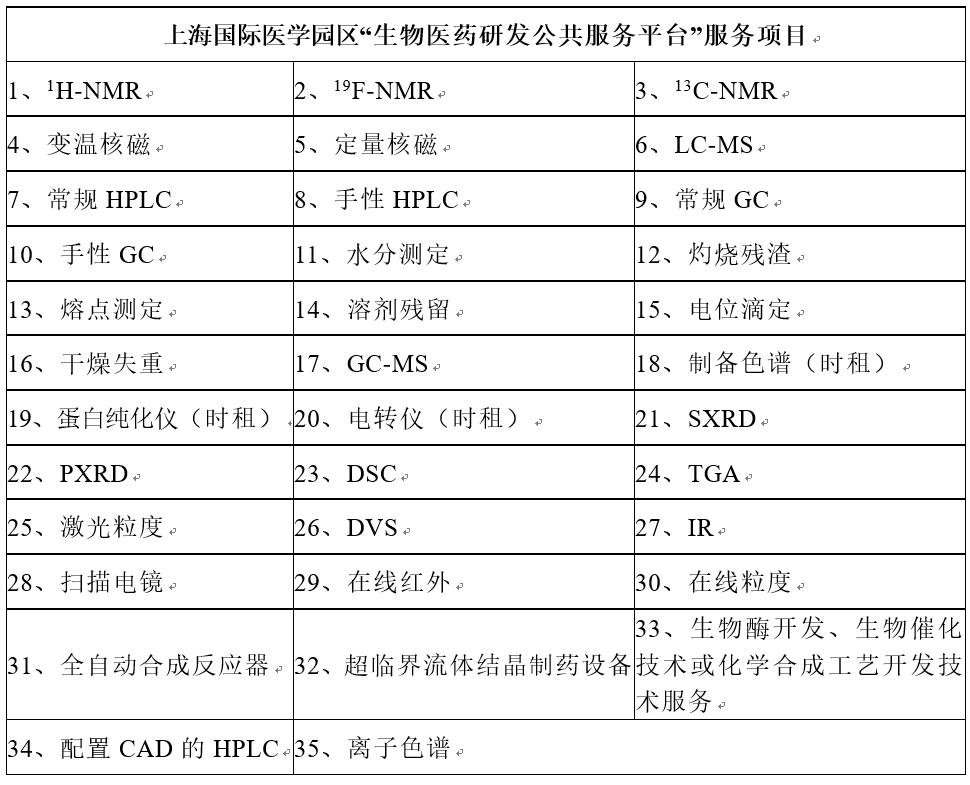
平台升级建设 | 国际医学园区研发公共服务平台实验室CNAS认可建设正式启动
CNAS为中国合格评定国家认可委员会(China National Accreditation Service for Conformity Assessment,CNAS)的英文缩写,是在原中国认证机构国家认可委员会(CNAB)和中国实验室国家认可委员会(CNAL)基础上合并重组而成的,CNAS是根据《中华人民共和国认证认可条例》的规定,由国家认证认可监督管理委员会(英文缩写为:CNCA)批准成立并确定的认可机构,统一实施对认证机构、实验室和检验机构等相关机构的认可工作。
Read more >>
生物催化系列酶介绍之一 — 酮还原酶
酮还原酶(KetoReductase,简称KRED),也称为羰基还原酶,是具有催化醛/酮与醇之间可逆氧化还原反应的酶类,需要NAD(H)或NADP(H)等辅酶作为氢传递体。
Read more >>
预告 l 尚科生物即将参展2022API China
第88届中国国际医药原料药/中间体/包装/设备交易会(API China)将于2022年11月9日-11日在青岛世博城国际展览中心举行。API China-专注于提高中国医药原料药、中间体、药用辅料生产、研发的整体水平,代表中国制药工业新产品和技术,已成为汇集行业内领军人物、展示先进的产品技术、为企业解读政策法规,提高行业生产水平并反映行业发展趋势的品牌盛会。
Read more >>
上一页
1
2
3
下一页
×
搜索


版权所有©尚科生物医药(上海)有限公司 沪ICP备09012407号  沪公网安备31011502015262号
沪公网安备31011502015262号
 沪公网安备31011502015262号
沪公网安备31011502015262号
×
-
-